
- Pengarang Miles Stephen stephen@answers-science.com.
- Public 2023-11-26 05:38.
- Terakhir diubah 2025-01-22 17:02.
Konfigurasi kulit terluar dari Arsenik adalah 4s24p3 jadi kulit terluarnya memiliki 5 elektron , sehingga membuat 5 elektron valensi . Jenis ikatan atom apa yang ada ketika elektron valensi adalah bersama?
Jadi, berapa banyak elektron valensi yang dimiliki arsenik?
5 elektron valensi
Juga, berapa banyak elektron valensi yang dimiliki golongan 5? Atom golongan 5 memiliki 5 elektron valensi. Atom golongan 6 memiliki 6 elektron valensi. Atom golongan 7 memiliki 7 elektron valensi.
apa satu-satunya logam dengan 5 elektron valensi?
Unsur-unsur golongan 15 (kolom) VA dari tabel periodik semuanya memiliki konfigurasi elektron s2p3, memberi mereka lima elektron valensi. Elemen-elemen ini termasuk Nitrogen (N), Fosfor (P), Arsenik (Sebagai), Antimon (Sb) dan Bismut (Dua).
Apa cangkang valensi arsenik?
Arsenik memiliki 5 elektron valensi . Itu terluar kerang (4s dan 4p) memiliki 5 elektron , ini adalah elektron valensi.
Direkomendasikan:
Apa konfigurasi elektron valensi inti untuk nitrogen?
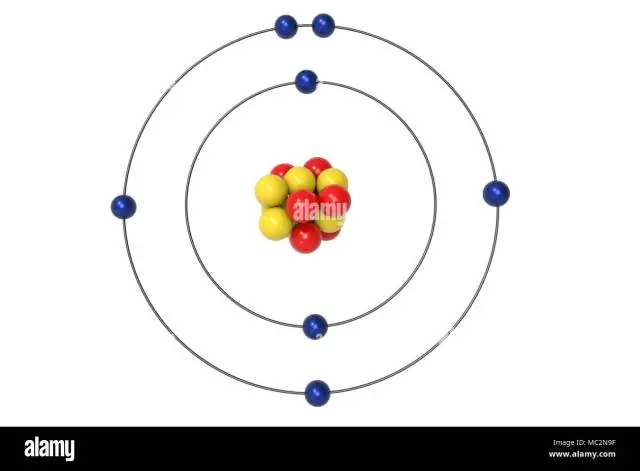
Tiga elektron yang tersisa akan masuk ke orbital 2p. Oleh karena itu konfigurasi elektron N akan menjadi 1s22s22p3. Notasi konfigurasi untuk Nitrogen (N) memberikan cara mudah bagi para ilmuwan untuk menulis dan mengkomunikasikan bagaimana elektron diatur di sekitar inti atom Nitrogen
Berapa banyak elektron valensi dalam atom netral astatin di?

Tujuh elektron valensi
Berapa banyak proton neutron dan elektron yang dimiliki arsenik?

Diagram komposisi nuklir dan konfigurasi elektron atom arsenik-75 (nomor atom: 33), isotop paling umum dari unsur ini. Inti atom terdiri dari 33 proton (merah) dan 42 neutron (biru). 33 elektron (hijau) mengikat nukleus, berturut-turut menempati kulit elektron yang tersedia (cincin)
Apakah semua semikonduktor memiliki 4 elektron valensi?

Kebanyakan konduktor hanya memiliki satu elektron di kulit valensi. Semikonduktor, di sisi lain, biasanya memiliki empat elektron di kulit valensinya. Masing-masing dari empat elektron valensi di setiap atom silikon dibagi dengan satu atom silikon tetangga. Jadi, setiap atom silikon terikat dengan empat atom silikon lainnya
Karakteristik atom logam mana yang membantu menjelaskan mengapa elektron valensi dalam logam terdelokalisasi?

Ikatan logam adalah pembagian banyak elektron yang terlepas di antara banyak ion positif, di mana elektron bertindak sebagai 'lem' yang memberi substansi struktur yang pasti. Ini tidak seperti ikatan kovalen atau ion. Logam memiliki energi ionisasi yang rendah. Oleh karena itu, elektron valensi dapat terdelokalisasi di seluruh logam
